Your basket is currently empty!
ProScern® – Chinese
ProScern® CFSE DC-T 细胞增殖检测
比较全蛋白抗原性的最佳方法
高度灵敏且多功能的 ProScern® DC-T 细胞检测可测量候选蛋白是否诱导辅助 CD4+ T 细胞增殖,这可能导致抗药抗体反应或其他不需要的免疫原性。
CD4+ T 细胞增殖通过流式细胞术使用 CFSE 染料稀释进行测量,CFSE 染料稀释是细胞增殖的一种敏感指标。
测定中使用完整配制的蛋白质,这提供了蛋白质的相对潜在抗原性的极好体外比较。
ProScern® DC-T 细胞检测结果的重要发表
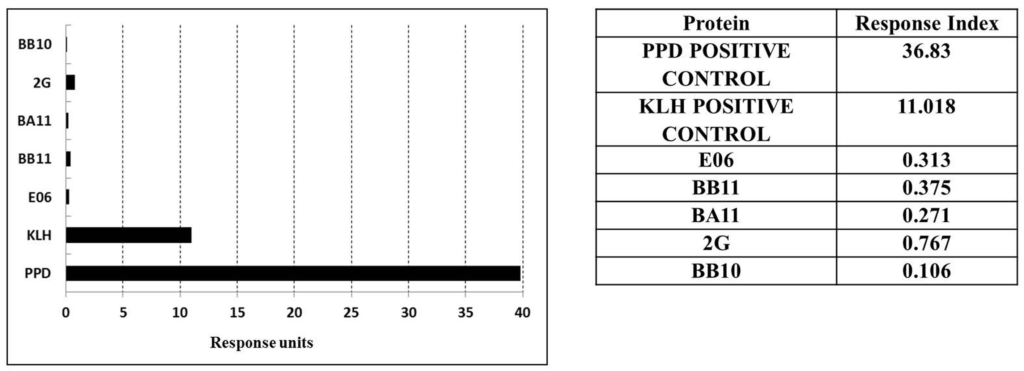
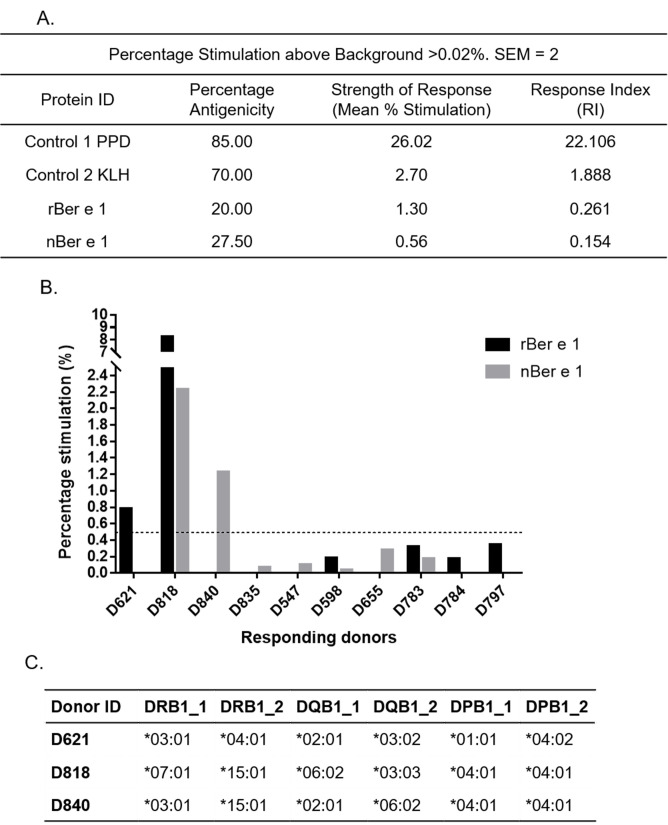
Figure 2: rBer e 1 和 nBer e 1 通过 DC-T 细胞反应测定的体外抗原性。 (A.) rBer e 1、nBer e 1 和参考蛋白的反应指数 (RI) 值来自抗原性百分比和刺激数据(高于背景的刺激百分比 ≥ 0.02%,SEM = 2) (B.) 反应供体的百分比图用 nBer e 1 和 rBer e 1 刺激后刺激超过 0.02% (SEM = 2)。虚线表示较高的刺激截止值 0.5% (C.) DRB1、DQB1 和 DPB1 等位基因谱表当用 rBer e 1 或 nBer e 1 刺激时,较高的刺激截止值≥0.5% (SEM = 2)。高于此截止值的刺激百分比表明抗原反应的意义更大。 (改编自原图)
在这篇简短的感言中,卫材 (Eisai) 的 Peng Li 博士描述了他与 ProImmune 合作使用 ProScern® DC-T 细胞增殖测定进行先导抗体选择的经验。
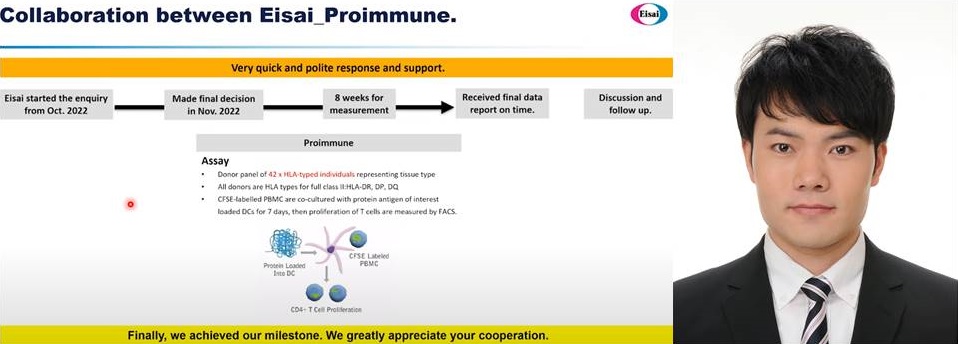
ProScern® DC-T 细胞检测用于全蛋白免疫原性筛选
用于筛选全蛋白的 ProScern® 树突状细胞 (DC)-T 细胞检测具有广泛的应用。它允许在临床前阶段对任何数量的候选药物的 T 细胞驱动的抗原性进行全面比较。至关重要的是,它还可以用于评估蛋白质序列以外的其他因素对抗原性的影响。这些差异可能包括比较生物仿制药、蛋白质修饰、降解产物、联合治疗中给出的化学实体,以及与制造工艺、赋形剂、药物配方和稳定性相关的其他参数。
此外,在某些情况下,可能无法直接使用抗原刺激 PBMC,特别是如果所涉及的抗原改变了响应 T 细胞的功能。为了避免这种测定干扰,可以使用树突细胞呈递抗原,从而可以直接比较不同先导物的相对抗原性。
ProScern® DC-T 细胞检测方法概述
该检测使用来自 ProImmune 健康高分辨率 MHC II 类组织分型供体样本库的样本。可以选择供体群组来提供对特定目标人群的代表性覆盖,或模拟在全球人群中发现的等位基因频率。通常使用 40 到 50 名捐赠者的队列,具体取决于研究的所需规模。
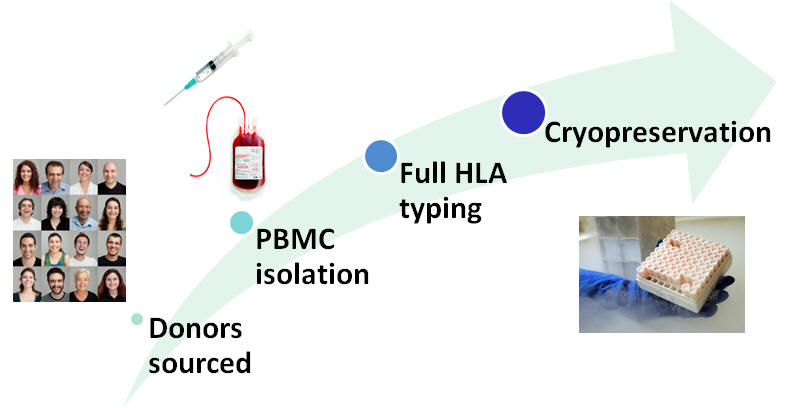
供体 PBMC 用作单核细胞的来源,在确定的培养基中培养以产生未成熟的树突细胞。 树突状细胞装载有测试抗原(全蛋白),然后通过在特定培养基中进一步培养被诱导成更成熟的表型。来自同一供体样品的 PBMC 用 CFSE 标记,然后与抗原引发的 DC 一起培养 7 天。每个 DC-T 细胞培养物包括一组未经处理的对照孔。该测定还包括参考抗原对照,包括两种有效的全蛋白抗原。
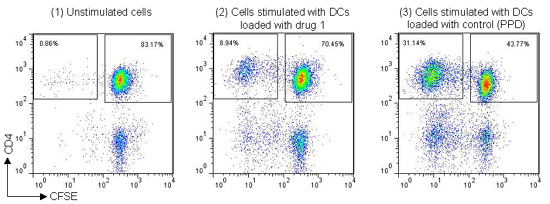
Figure 3. 来自 DC-T 细胞测定的示例染色数据,(1) CFSE 标记的 T 细胞与未与抗原共培养的 DCs 一起孵育,(2) CFSE 标记的 T 细胞与之前与全蛋白抗原共培养的 DC 一起孵育 (Drug 1), (3) CFSE 标记的 T 细胞与之前与对照抗原共培养的 DC 一起孵育 (Tuberculin PPD)。
评估免疫原性的反应指数
在评估免疫原性时,应考虑整个研究队列中供体细胞反应的频率。2 个或更多独立供体样本中的阳性反应(高于背景的刺激百分比 > 0.5%)被认为是潜在的体内 T 细胞反应的指标。考虑阳性供体细胞反应的强度也很重要。这是通过对每种药物在接受的供体中获得的高于背景的刺激百分比取平均值来确定的。反应指数是通过将反应强度的值乘以供体反应的频率来计算的。与仅依赖反应频率的分析方法相比,该指数更能代表免疫原性水平。
如果在两种 T 细胞检测中的任何一种中都观察到供体样本中的阳性反应,则表明增殖性免疫反应已经通过该供体提供的六个 HLA II 类等位基因中的至少一个产生。
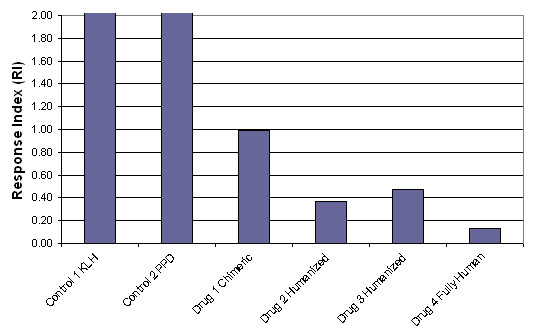
Figure 4. 使用 40 名供体和 4 种测试蛋白(在本例中为治疗性抗体)和 2 种对照进行的 DC-T 细胞测定的结果。
如 Figure 4 所示,完全人源抗体药物 4 的反应指数最低,表明 ProScern® DC-T 细胞检测的体外免疫原性最低。正如预期的那样,人源化抗体(Drug 2 和 Drug 3)显示出次低的免疫原性,而嵌合抗体(Drug 1)显示出最高的免疫原性。不同的治疗蛋白会产生特定水平的免疫原性,这可以在 ProImmune DC-T 细胞检测中直接量化。
ProImmune 在树突状细胞培养方面的专业知识
通过开发我们的 ProScern® DC-T 细胞增殖检测和我们的 ProPresent® 抗原呈现检测,我们在处理树突细胞方面拥有丰富的专业知识。如果您需要依赖于这些技能的检测,请联系我们,看看您是否可以从与我们合作中受益:我们的特殊检测服务可能会对您的研究计划产生影响。
